Zoom in auf die neuronale Verhalten

Es gibt mehr als 86 Milliarden Neuronen im Gehirn. Diese Zellen kommunizieren durch das senden von elektrischen und chemischen Signalen über Wege und sind verantwortlich für die Kontrolle alles, von der einfachen Bewegung bis hin zur Verarbeitung und Speicherung von komplexen Gedanken und Erinnerungen. Die schiere Ungeheuerlichkeit dieser neuronalen Netzwerk macht das Gehirn eine schwierige Grenze für die exploration, aber Michael Tadross und Yiyang Gong, zwei Fakultät der Duke University Department of Biomedical Engineering und Empfänger der NIH Young Innovator Award, mit unterschiedlichen Ansätzen zu entschlüsseln, die Körper der komplexeste organ.
Eine molekulare GPS zum Ziel Neuronen
Michael Tadross, MD, ist assistant professor in Duke BME, wo sein Labor verwendet eine neuartige Technologie, genannt DART, Drogen oder Akut Eingeschränkt durch Tethering, der Lieferung von Arzneimitteln an bestimmte Zellen im Gehirn. Durch die Nutzung von DART, Tadross und sein Labor hoffen, ein besseres Verständnis dafür entwickeln, wie Medikamente wirken im Gehirn.
„Drogen haben schon wirklich wichtig in der Geschichte der Neurowissenschaft und der neuropsychiatrische Erkrankung, und ich denke, wir nehmen es für selbstverständlich, dass die Gehirn-Erkrankungen sind biologische Krankheiten. Es gab eine Zeit, das war nicht weit geglaubt, um wahr zu sein“, sagt Tadross. „Der Wendepunkt kam in den 1950er Jahren, nachdem die Medikamente wurden zufällig entdeckt zu haben, eine Wirkung auf Erkrankungen wie Depressionen.“
Diese Entdeckung löste eine Rasse zu entdecken genau das, was diese Medikamente sind verbindlich in das Gehirn, mit dem Ziel, ein besseres Verständnis die Grundlage der Erkrankung des Gehirns. Mehr als 60 Jahre später, können Forscher immer noch fehlt, ist das tiefere Verständnis.
Aber DART konnte diese lange stehenden Fragen durch die Aktivierung Tadross und sein team zum Ziel Drogen zu einer Art von neuron zu einer Zeit.
Drogen sind heute nicht in der Lage, zu unterscheiden zwischen verschiedenen Gruppen von Zellen. Zum Beispiel, wenn jemand behandelt wird für eine Stimmung-Verwandte Störung wie der depression, die Ihnen verschrieben werden ein Medikament namens ein SSRI. Diese Medikamente Zielen auf einen rezeptor, resorbiert der Botenstoff serotonin, ein neurotransmitter, der eine Rolle spielt in der Stimmung. SSRIs blockieren diese Rezeptoren und fördern so die Menge an serotonin im Gehirn.
Das problem bei diesem Ansatz ist, dass es Tausende oder gar Millionen von Zellen, die Ausdruck der gleichen rezeptor, so dass, wenn Sie nehmen ein Medikament, es wirkt sich auf alle Zellen in der gleichen Zeit, führt Häufig zu einer komplexen Reihe von Effekten. Während SSRIs, zum Beispiel, können effektiv zu behandeln depression, können Sie auch einen negativen Effekt auf Angst.
„Es ist schon eine Menge Arbeit zugeschnitten in Richtung lokal Infusion von Medikamenten in bestimmte Teile des Gehirns, wie der amygdala oder der präfrontale cortex“, sagt Tadross. „Aber DART ermöglicht es Ihnen, das zu tun, zu einem weit größeren Grad an Spezifität.“
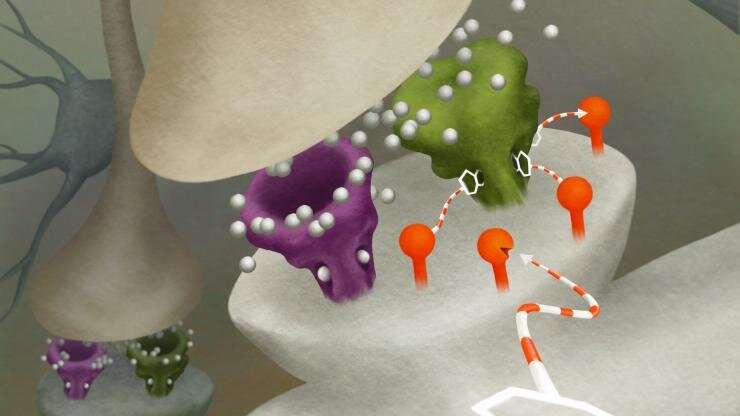
DART-Werke von gentechnisch Programmierung spezifischer Zelltypen zu äußern, ein virus, der wirkt wie ein GPS-Leuchtfeuer. Dieser Leuchtturm, der aus einem protein in Bakterien gefunden, Mäntel die Oberfläche von target-Zellen, und zieht Drogen geladen mit einer speziellen homing-Gerät. Wenn ein Medikament in das system eingebracht, es ist gefangen von diesem Leuchtturm und schafft eine lokal hohe Konzentration der Droge.
„Es ist ein universal-aus-Schalter für jedes Medikament, und das ist die Dosis“, sagt Tadross.
„Der homing-Gerät und GPS-beacon sind so effizient, dass die Konzentration des Medikaments auf die Zellen von Interesse akkumuliert zu werden 1000 mal höher als irgendwo sonst innerhalb von wenigen Minuten, so dass es nur wirkt, wo Sie es wollen. Die Einfachheit dieser Idee ermöglicht es, arbeiten für praktisch jede Droge.“
Tadross und sein Labor mit DART zu entwirren die Geheimnisse des menschlichen Gehirns, beginnend mit Bewegungsstörungen wie der Parkinson-Krankheit. Das team hat sich darauf konzentriert, Ihre Anstrengungen auf das striatum, einer Struktur in den Basalganglien, die hilft bei der Kontrolle der Rede, der Bewegung und der Körperhaltung. Unter den verschiedenen Zelltypen im striatum sind D1-und D2-Zellen, die eng vermischt, sondern kommunizieren auf verschiedene Regionen des Gehirns.
In Parkinson-Modellen, die Zellen, die den neurotransmitter Dopamin produzieren beginnen zu sterben ab, wodurch weniger Dopamin gesendet werden, in den Basalganglien. Zum Ausgleich für diese Verringerung von Dopamin in Verbindung steht, das Gehirn versucht, rewire sich durch die Veränderung der Signale durchgeführt, die durch den Botenstoff Glutamat, wodurch ein Ungleichgewicht.
Um die Rolle von Glutamat bei der Parkinson-Krankheit, Tadross und seinem Labor arbeitete mit einem Parkinson-Modell der Maus. Diese Tiere haben Schwierigkeiten beim bewegen, entwickeln eine gekrümmte Haltung, und die kann nur in eine Richtung. Anstatt zu behandeln die Störung durch die Erhöhung Dopamin (die standard-Behandlung), die Sie verwendet, DART beenden die D2 Typ der Nervenzelle von der Kompensation durch die Bereitstellung einer Glutamat-antagonist spezifisch an diese Zellen in das striatum. Das Tier die Bewegung dramaticallyimproved. Bemerkenswert ist, dass diese Verbesserung war nur zu sehen, wenn die Droge war darauf ausgerichtet, ausschließlich auf D2-Zellen; liefern das Medikament sowohl D1-und D2-Zellen hatte keinen nutzen.
„Zuerst waren wir überrascht zu sehen, wie eine dramatische Wirkung, da wir wussten, dass Glutamat-Antagonisten wurden in der Vergangenheit noch nie gearbeitet, zur Behandlung von Morbus Parkinson. Im Nachhinein machte es Sinn. Man kann sich das wie eine Wippe, wo es ein Ungleichgewicht in der Schaltung; targeting ein Medikament nur auf eine der Zellen ist eine großartige Möglichkeit, um eine bessere Ausgewogenheit der Wippe“, sagt Tadross. „Es sind noch viele Fragen zu beantworten, und wir sind jetzt mit neuer DARTs zu untersuchen, wie unterschiedliche Neurotransmitter tragen zu dieser Störung.“
Darüber hinaus untersuchen von Bewegungsstörungen, Tad ross und sein team sind daran interessiert, die Verwendung des DART-Studie zu Themen wie sucht, vor allem in Bezug auf Opioide. Im Jahr 2018 allein in den Zentren für Disease Control and Prevention berichtet, dass mehr als 68.000 Menschen starben von Drogen-überdosierungen in den Vereinigten Staaten, und Opioide waren verantwortlich für einen Großteil dieser Todesfälle. Das Tadross lab hofft, mit Ihrer Technologie zu untersuchen, welche Zellen im Gehirn sind die meisten hilfreich für die Linderung der Schmerzen und die Zellen fahren sucht.
„Jedes Medikament hat einige gute Dinge und schlechte Dinge mit ihm verbunden, doch während es noch nicht ein weiteres Medikament, das in der Lage ist, entsprechen die Schmerzlinderung Vorteile der Opioide, diese Medikamente so gefährlich sind und süchtig machen, dass Ihre Kosten überwogen haben Ihre Vorteile“, sagt Tadross. „Unsere Hoffnung ist es, DART -, um besser zu verstehen, wie können wir die Schmerzen zu lindern, ohne dabei die negativen Nebenwirkungen.“
„Würde nicht es groß sein, um zu verstehen, wie Sie funktionieren und schließlich entwickeln eine Therapie, die entworfen wurde, auf den Einsatzzweck eher als versehentlich?“, fragt Tadross. „Wir wissen nicht, die Antworten auf diese großen Fragen, aber wir haben jetzt die Werkzeuge, die weisen uns in die richtige Richtung.“
Die Beleuchtung der Gehirnaktivität
Wenn Yiyang Gong beschreibt, hat lab als interdisziplinäre, er ist nicht übertrieben. Sein team schafft Werkzeuge, die an dem Schnittpunkt von Neurobiologie, Optik und engineering. Gong ist ein Assistent professor an der Duke University ‚ s Department of Biomedical Engineering, und sein Labor Studien Gehirn schaltungen, die durch die Aufnahme, störende und Steuern die Aktivität des Gehirns in verschiedenen Situationen.
„Unser Ziel ist das aufzeichnen von neuralen Aktivitäten in neuen Möglichkeiten“, sagt Gong. „Unser Labor verwendet fächerübergreifende Methoden und Techniken zu verstehen, wie Neuronen miteinander kommunizieren. Wir erreichen dies mit Hilfe von sensoren, die wir entwickelten, dass flash in Antwort auf neuronale Signale, und die Paarung, die mit Mikroskopie-tools, die uns helfen, aufzeichnen, blinkt diese.“
Die Neuronen erzeugen und kommunizieren von Nachrichten teilweise durch Veränderung Ihrer Spannung. Diese elektrischen Signale können gemessen werden, wie einzelne Impulse von einem neuron genannt, ein aktionspotential, oder als oszillierende Wellen der Aktivität einer Gruppe von Neuronen, die zusammen arbeiten.
Gong und seine Labor entwickelt, Spannungs-sensoren aus DNA-Stücke, die können geliefert werden, um target-Neuronen mit einem virus. Sobald das virus vorhanden ist, die DNA kodiert für ein protein, das sitzt auf der Zellmembran und blinkt in Reaktion auf die Nervenzelle verändert sich die Spannung. Durch die genetisch auf verschiedene Typen von Neuronen mit seinem sensor -, Gong Hoffnungen zu verstehen, wie diese Zelltypen schwingen zusammen und dazu beitragen, verschiedene Arten von Gehirnwellen.
Seit Ihrer Gründung Gong hat in der Lage gewesen, diese sensoren in Zellkulturen und intakten Geweben und sogar live-Tier-Modelle. Nun, das Labor zielt auf die Verbesserung dieser sensoren sowohl durch die Erhöhung Ihrer Geschwindigkeit und dividieren Sie durch die Einführung von mehreren Farben.
„Dieser zweite Punkt ist besonders wichtig, denn wir würden gern sehen, wie neuron 1 neuron kommuniziert mit 2, oder wie Bevölkerung 1 kommuniziert mit Bevölkerung 2,“, sagt Gong. „Diese Erkenntnisse könnten helfen, enthüllen die neuronalen Ursprung von komplexen Handlungen wie lernen, erinnern und Entscheidungsprozesse.“
Neben der Entwicklung dieser genetischen sensoren, Gong und seinem team zu erforschen, wie Sie können, Voraus-Mikroskopie-tools zu erfassen blinkt. Bisher haben Wissenschaftler Werkzeuge entwickelt, die Messen kann, ein paar aktionspotentiale einer Sekunde. Laut Gong, es war kein schieben, um die Geschwindigkeit des imaging-tools, weil das so schnell wie herkömmliche optische sensoren, die neuronale Aktivität reagiert haben.
„Mit der Einführung der genetisch kodierte Spannung sensoren, die wir auch entwickeln musste wirklich schnell-Mikroskopie auf den gleichen Zeitskalen“, sagt Gong. „Unser Ziel ist die Entwicklung schneller Versionen von Fluoreszenz-mikroskopen, die können noch Bild-große Teile des Gehirns.“
Die Gong-Labor arbeitet auch an neuen Methoden zur Unterstützung bei der Bearbeitung von eingehenden Daten. In Zusammenarbeit mit Sina Farsiu, die Paul Ruffin Scarborough Associate Professor of Engineering an der Duke, Gong entwickelt hat, ein automatisierter Prozess, kann schnell die Erfassung und Verarbeitung neuronaler Signale für die Echtzeit-Verhaltens-Studien.
Derzeit identifizieren Neuronen, die in den Aufnahmen ist ein mühsamer Prozess. Die Genaueste Methode beinhaltet ein menschlicher analyst Kreisen jeder „spark“ Sie sehen, in einer Aufnahme, oft erfordert Sie zu stoppen und Spulen Sie das video bis jeder gezielte neuron identifiziert wurde. Dieser Prozess, das sogenannte Segmentierung, ist anspruchsvoll und zeitaufwendig, und ein Forscher verbringen kann überall von vier bis 24 Stunden Arbeitszeit eine 30-minütige Aufzeichnung.
Aber der neue Algorithmus entwickelt von Gong und Farsiu genau zu identifizieren und zu segmentieren Neuronen in wenigen Minuten. „Die Daten Analysten haben verbrachte Stunden und Stunden Minuten Verarbeitung von Daten, und erstellt einen Engpass in der Neurowissenschaft ist das ein problem für eine lange Zeit. Aber unser Algorithmus verarbeiten kann ein 30-minütiges video, in 20 bis 30 Minuten“, sagt Gong. „Wir waren auch in der Lage, zu generalisieren und seine Leistung, so kann es funktionieren ebenso gut, wenn wir brauchen, um segment Neuronen aus einer anderen Ebene des Gehirns mit unterschiedlichen neuron Größe oder dichten.“
Gong ist bereits mit dieser neuen Technik zur Untersuchung der Beziehung zwischen neuronaler Aktivität und verschiedenen Verhaltensweisen bei Mäusen. Durch das Verständnis, welche Neuronen feuern, die während bestimmter Aktivitäten, seinem Labor lernen konnten, wie die Forscher manipulieren können, die Aktivität des Gehirns Verhalten zu ändern.